Quel trapianto fatto a cuore pulsante – Di Nadia Clementi
Riportiamo l'intervista fatta due anni fa al prof. Gino Gerosa, di origini roveretane, che è diventata decisamente attuale dopo il successo innovativo nel trapianto di cuore
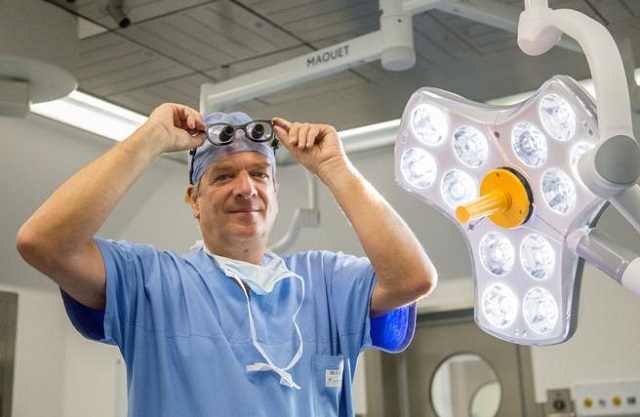
Il prof. Gino Gerosa.
In
Italia, lo scompenso cardiaco determina ogni anno la morte di 150mila
persone, circa 800 sono in lista d'attesa di trapianto e solo 250 sono i
pazienti trapiantati.
Ad oggi la morte cerebrale post traumatica si è
quasi azzerata e i donatori d’organo sono sempre più vecchi, a questo
si aggiunge che in Italia per stabilire una morte cardiaca è previsto un
elettrocardiogramma piatto per 20 minuti, rispetto ai 5 minuti del
mondo anglosassone, tutto quanto rende molto difficile utilizzare il
cuore per il trapianto.
Vista la difficoltà a reperire organi e la
mancanza di donatori, il cuore artificiale rappresenta la nuova cura per
il futuro, capace di prolungare la vita dei malati in stadio avanzato
di insufficienza cardiaca.
Pur sapendo che la migliore soluzione
resta il trapianto di organi da donatore umano, sia per aspettativa che
per qualità di vita, l’attuale situazione necessità di trovare con
urgenza delle valide alternative.
In prima linea, su questo
fronte, troviamo l’illustre professor Gino Gerosa, cardiochirurgo di
fama mondiale, che per il 2022, grazie anche al sostegno del Pnrr, conta
di trovare i finanziamenti per realizzare due importanti progetti: uno
per la creazione di un cuore bionico tutto italiano unisex (di
dimensioni più piccole rispetto a quello attuale) e l’altro è quello di
prendere un cuore animale, decellularizzarlo, vale a dire rimuovere
tutte le cellule, e ripopolarlo con le staminali del potenziale
ricevente.
Per la realizzazione di questi progetti sarà
indispensabile la collaborazione tra diversi poli di eccellenza.
Fortunatamente, l’Italia è un hub di ingegneri con le più alte
qualifiche, come per esempio Leonardo, Ferrari e Cibio.
Ancora una
volta dunque, la cardiochirurgia padovana tra i Centri di ricerca più
all’avanguardia del mondo, dimostra la sua valenza e professionalità e
apre la strada ad una nuova possibilità d'intervento che potrà rendere
letteralmente la vita a molte persone le quali, a causa della loro
condizione, la devono percorrere costantemente in salita.

Il gruppo del reparto.
Noi
per saperne di più abbiamo intervistato il prof. Gino Gerosa, Direttore
del Centro di Cardiochirurgia e del Programma Trapianto di Cuore e
Assistenza Meccanica dell’Azienda Ospedale-Università di Padova e
Professore Ordinario di Cardiochirurgia del Dipartimento di Scienze
Cardio- Toraco-Vascolari e Sanità Pubblica dell’Università di Padova.
È
stato il primo cardiochirurgo in Italia ad eseguire un intervento di
rivascolarizzazione miocardica a cuore battente nel 2001 usando il
sistema robotico Da Vinci e, nel 2004, il primo intervento di isolamento
delle vene polmonari per il trattamento della fibrillazione atriale
sempre con il sistema robotico Da Vinci.
Nel marzo 2002 ha
effettuato la prima applicazione clinica di cellule staminali autologhe,
come terapia per l'insufficienza cardiaca.
Nel 2007 ha eseguito il
primo impianto in Italia, di un cuore artificiale totale CardioWest 70
cc. Nel 2015, per la prima volta al mondo, ha eseguito l'impianto di un
cuore artificiale, di dimensioni ridotte «CardioWest 50cc» su un ragazzo
di 26 anni affetto da un linfoma e già trapiantato di cuore. Il primo
di molti altri.
Il prof. Gerosa è nato a Rovereto nel 1957, vanta una
lunga esperienza professionale all’estero e, tra i vari riconoscimenti
ottenuti, è stato insignito, nel 1993, del prestigioso Alexis Carrel
Award, dedicato all'omonimo premio Nobel per la Medicina.
Chi è il prof. Gino Gerosa  Curriculum breve Curriculum breve - Professore Ordinario di Chirurgia Cardiaca Università degli Studi di Padova dal novembre 2015 - Direttore U.O. Cardiochirurgia, Azienda Ospedaliera di Padova, dal febbraio 2003 - Direttore Centro Trapianti e Programma Assistenza Meccaniche al Circolo dal 2003 - Direttore Scuola di Specializzazione in Cardiochirurgia – Università degli Studi di Padova (dal 2003 – al 2013) - Direttore Scientifico CORIS - Consorzio per la Ricerca Sanitaria della Regione Veneto (dal 2016) - Coordinatore del Dipartimento Funzionale Organi Artificiali e Medicina Rigenerativa dell’ Azienda Ospedale-Università di Padova (dal 2019) Ha eseguito il primo intervento in Italia di rivascolarizzazione miocardica a cuore battente con sistema robotico Da Vinci. (First italian robot enhanced coronary bypass Ital Heart J 2004 Jun; 5 (6) 475-8). Ha eseguito il primo intervento in Italia di isolamento delle vene polmonari totalmente endoscopico con il sistema robotico Da Vinci (Totally endoscopic robotic-guided pulmonary veins ablation: an alternative method for the treatment of atrial fibrillation Eur J Cardiothorac Surg 2004 Aug: 26 (2): 450-2). Ha eseguito intervento di rivascolarizzazione miocardica e endoarterectomia carotidea in pazienti sveglio (Simoultaneous coronary artery by-pass grafting and carotid endarterectomy in an awake Jehova’s witness patient without endotracheal intubation. Eur J Cardiothorac Surg 2005 Jan; 27 (1): 168-170). Ha eseguito il primo impianto in Italia di assistenza ventricolare sinistra con Berlin Heart Incor (2003). Ha eseguito uno dei primi trapianti al mondo di cellule staminali in paziente affetto da miocardiopatia post-ischemica nel 2002. Ha diretto l’equipe che ha eseguito il primo trapianto cardiaco ABO incompatibile in Italia in paziente pediatrico (2006) (ABO-incompatible heart transplantation: crossing the immunological barrier. J Cardiovasc Med (Hagerstown2008 Aug; 9 (8): 854-7). Ha eseguito il primo impianto in Italia del cuore artificiale totale Cardiowest (2007). Nel settembre 2011 ha eseguito con successo il trapianto di cuore nel paziente con la più lunga sopravvivenza al mondo con un cuore artificiale totale (3 anni e 8 mesi). Nel 2015 ha eseguito il primo intervento al mondo di sostituzione valvolare aortica combinato ad una plastica valvolare mitralica senza l’utilizzo della circolazione extracorporea ed a cuore battente attraverso l’apice del ventricolo sinistro. Nell’aprile 2015 ha eseguito per la prima volta al mondo l’impianto di un cuore artificiale totale Cardiowest 50 cc in un ragazzo già trapiantato di cuore. Nel maggio 2016 ha eseguito per la prima volta al mondo, in un paziente affetto da insufficienza mitralica, l’impianto di un anello mitralico senza l’utilizzo della circolazione extracorporea ed a cuore battente attraverso l’apice del ventricolo sinistro. Sotto la sua guida il Centro di Cardiochirurgia di Padova è diventato il primo Centro in Italia per numero di trapianti cardiaci e impianti di sistemi di assistenza ventricolare (cuori artificiali) nel 2015. Il Laboratorio di Ricerca di Medicina Rigenerativa da lui fondato e diretto ha messo a punto la tecnologia per decellularizzare la valvola cardiaca umana (homograft) da utilizzare nei pazienti pediatrici e cardiopatici congeniti adulti. Tale tecnologia è stata donata alla Banca del Tessuti di Treviso che risulta oggi l’unica Banca dei Tessuti in Europa oltre ad Hannover ed essere proprietaria di tale tecnologia. È autore di più di 400 pubblicazioni scientifiche e co-autore di 8 libri di interesse cardiochirurgico. |
Professor Gerosa cos’è un cuore artificiale e come funziona?
«Possiamo
suddividere i sistemi di assistenza meccanica al circolo in VAD
(sistemi di assistenza ventricolare) che sostituiscono la funzione di un
solo ventricolo, in genere il sinistro, con il cuore del paziente che
resta in sede e viene applicato il VAD al ventricolo disfunzionante.
«Il
cuore artificiale totale si utilizza negli scompensi bi-ventricolari ed
è un vero e proprio trapianto nel senso che il cuore del paziente viene
rimosso e sostituito dal cuore meccanico.
«Al momento ne esistono
due modelli: uno pneumatico, nordamericano, costituito da due gusci di
poliuretano che rappresentano i ventricoli con all’interno una membrana
di poliuretano che viene movimentata dall’aria compressa prodotta da un
compressore in modo da espellere il sangue dai ventricoli nel circolo
sistemico e polmonare.
«È molto semplice dal punto di vista tecnico
ma estremamente rumoroso. Il secondo, prodotto in Francia, è alimentato
da un motore elettrico che attiva due piccole pompe che spostano un
fluido (silicone) che alternativamente movimenta due membrane che
espellono il sangue dai ventricoli nel circolo sistemico e polmonare.
«A
differenza del cuore pneumatico è silenzioso ma con un ingombro elevato
tanto che meno del 75% degli uomini e meno del 25% delle donne possono
essere potenziali riceventi.
« Entrambi i cuori sono alimentati da
batterie e da una unità di controllo che il paziente porta in cintura
nel caso del cuore francese, in uno zainetto assieme al compressore nel
cuore nordamericano.»
Foto del primo cuore artificiale totale impiantato in Italia a Padova nel 2007. Oggi esposto al MUSE.
Che differenza c’è tra cuore artificiale e cuore bionico?
«Il cuore, per così dire bionico,
ha il grande pregio di presentare parte dei componenti costituiti da
materiale biologico, ad esempio il rivestimento interno dei ventricoli
artificiali. Questo ottimizza l’emocompatibilità del sistema riducendo
la necessità di terapia anti-trombotica e permette la personalizzazione
del cuore per il singolo paziente (medicina personalizzata).»
Perché è importante arrivare al cuore artificiale unisex?
«Nell’ottica
della medicina di genere è importante sviluppare un cuore artificiale
di dimensioni il più possibile ridotte, in modo tale da ipotizzare
l’impiego in donne, uomini e adolescenti indipendentemente dalla taglia
corporea.
«Potrà poi essere personalizzato per il singolo paziente grazie alle tecniche di ingegneria tissutale.»

Fotografia di un cuore decellularizzato.
Ci spiega in cosa consiste il progetto di trapianto di cuore animale a un uomo?
«In
questo caso abbiamo due strategie terapeutiche: una più avveniristica
che consiste nel decellularizzare un cuore di maiale, ovvero rimuoverne
tutta la componente cellulare (cardiomiociti, cellule muscolari lisce,
cellule endoteliali) lasciando il solo scheletro di collagene ed
elastina: questo scaffold verrà poi ripopolato, successivamente, con le
IPS ovvero cellule staminali in cui è stata indotta la possibilità di
differenziarsi in diversi tipi cellulari. «Il cuore verrà dunque
ripopolato con le cellule del potenziale ricevente non necessitando di
terapia immunosoppressiva.
«La seconda strategia, utilizzata per la
prima volta nell’uomo qualche mese fa a Baltimora, negli Stati Uniti, è
rappresentata dallo xenotrapianto. In questo caso si trapianta il cuore
di un maiale geneticamente modificato in modo tale che non esprima più
gli antigeni responsabili del rigetto iperacuto. Questa tecnica
dev’essere ulteriormente raffinata per evitare, ad esempio, la
trasmissione di zoonosi dal maiale all’uomo ma rappresenta, al momento,
una potenziale opportunità terapeutica.»
Chi sono i pazienti che possono accedere al trapianto di cuore bionico?
«Tutti i pazienti affetti da scompenso cardiaco terminale che presentano una disfunzione bi-ventricolare.»
Ci parla della sua equipe medica?
«Tutto
quello che abbiamo prodotto in questi anni di assoluta eccellenza
cardiochirurgica, pensi che dal 2003 ad oggi abbiamo eseguito 6 primi
interventi al mondo e 14 primi interventi in Italia, sono ovviamente il
frutto di un lavoro di equipe, un lavoro di squadra: cardiochirurghi,
anestesisti, tecnici e infermieri che grazie alla loro abnegazione e
dedizione hanno reso l’impossibile possibile.»

A che punto siete con i progetti, futuro o realtà?
«Come
sempre accade nella ricerca, la possibilità di ottenere risultati
concreti e prontamente trasferibili in ambito clinico è strettamente
legata ai finanziamenti disponibili.
«Dobbiamo dunque sempre
scontrarci con supporti finanziari non sempre adeguati alla
realizzazione delle visioni traslazionali che ci caratterizzano.
«Stiamo dunque parlando di una realtà futuribile che potrebbe trovare rapida realizzazione.»
Quali sono, secondo lei, le prospettive future dell’utilizzo dell’innovazione in ambito sanitario?
«L’evoluzione
tecnologica è fondamentale per migliorare i percorsi assistenziali che
possiamo offrire ai nostri pazienti. Gli investimenti nelle nuove
tecnologie sanitarie non devono essere visti semplicemente come un costo
bensì come un’opportunità.
«Se penso all’ambito cardiochirurgico,
grazie all’innovazione tecnologica e al miglioramento delle tecniche,
siamo passati dalla chirurgia tradizionale alla chirurgia mini-invasiva a
quella microinvasiva ovvero la capacità di correggere le alterazioni
strutturali cardiache senza aprire il torace del paziente, utilizzare la
circolazione extracoprorea e fermare il cuore.
Questo grazie ai
nuovi device e alle tecnologie transacatetere con un enorme beneficio
per il paziente in termini di riduzione del dolore e di una più rapida
ripresa fisica.»
Nadia Clementi - [email protected]
Prof. Gino Gersosa - [email protected] - tel. 049- 8212410
https://www.dctv.unipd.it/dipartimento/sedi-e-strutture/strutture/cardiochirurgia









































